23批次中藥飲片不合格,暫停銷售使用、召回產品!
日期:2017/3/11
國家食品藥品監督管理總局3月9日發布關于23批次中藥飲片不合格的通告(2017年第39號)。
經河北省藥品檢驗研究院檢驗,標示為樟樹市慶仁中藥飲片有限公司等22家企業生產的23批次中藥飲片不合格。
經河北省藥品檢驗研究院檢驗,標示為河北聯康藥業有限公司、南京海源中藥飲片有限公司、安徽省金芙蓉中藥飲片有限公司、江西青春康源中藥飲片有限公司、樟樹市慶仁中藥飲片有限公司、山東鄄城志遠中藥飲片有限公司、河南千方藥業有限公司、禹州市凱旋藥業有限公司、禹州市金地中藥飲片有限公司、湖北神農本草中藥飲片有限公司、湖南福泰中藥飲片有限責任公司、邵陽神農中藥科技發展有限公司、廣西貴港市神農藥業有限公司、四川景程中藥飲片有限責任公司、甘肅省國草藥業有限公司、甘肅溫泉生物科技有限責任公司、青海九康中藥飲片有限公司等企業生產的23批次連翹不合格。
不合格項目包括含量測定、浸出物、雜質等(詳見下表)。
23批次不合格中藥飲片名單
(點擊圖片可放大觀看)
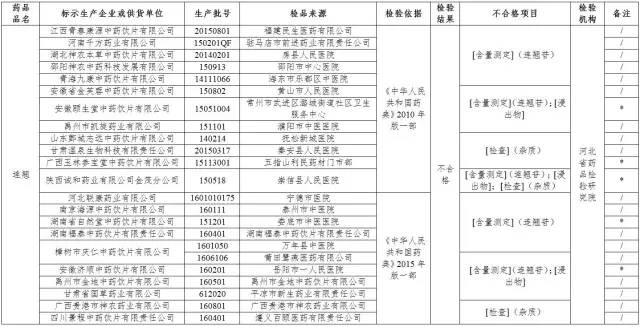
備注:標“*”的藥品為標示生產企業否認為該企業生產。
對上述不合格中藥飲片,相關省(區、市)食品藥品監督管理局已采取查封扣押等控制措施,要求企業暫停銷售使用、召回產品,并進行整改。
國家食品藥品監督管理總局要求生產企業所在地省(區、市)食品藥品監督管理局對上述企業依據《中華人民共和國藥品管理法》第七十三、七十四、七十五條等規定對生產銷售不合格產品的違法行為進行立案調查,三個月內公開對生產銷售不合格藥品相關企業或單位的處理結果,相關情況及時報告總局。
在立案調查工作中,企業對產品真實性有異議的,可以向所在地省(區、市)食品藥品監督管理局提出,由當地省(區、市)食品藥品監督管理局對企業生產銷售情況進行調查核實,并將情況通報被抽樣單位所在地省(區、市)食品藥品監督管理局。被抽樣單位所在地省(區、市)食品藥品監督管理局接到對不合格產品真實性異議的通報后,要立即立案調查,追溯產品來源。如確屬標示生產企業生產的,由相關省(區、市)食品藥品監督管理局對生產企業從重處罰。
信息來源:中國食事藥聞
|