重磅藥物赫賽汀專利臨期,CDE廣發“英雄帖”!
日期:2017/11/7
羅氏“王牌”原研藥——赫賽汀(曲妥珠單抗)專利即將到期,國家藥品審評中心(CDE)日前專門發文,征募、助力本土企業積極研制赫賽汀的生物類似藥。

上述《通知》是在CFDA已發布的《生物類似藥研發與評價技術指導原則(試行)》基礎上,針對曲妥珠單抗臨床研究策略,列出生物類似藥研發可能存在的兩種情況及應對策略,為本土藥企加快研發提供參考。
《通知》正在向申報機構、研究者等相關方面征求意見,為期1個月。CDE表示,必要時還將會組織會議,邀請各方積極參與討論。
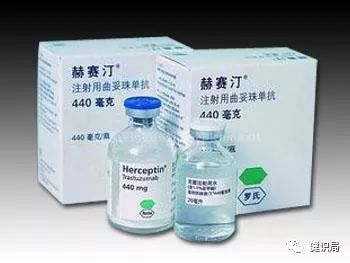
注射用曲妥珠單抗(商品名:赫賽汀)是由瑞士羅氏公司研發的一種重組DNA衍生的人源化單克隆抗體,可有效抑制腫瘤細胞的生長。
1998年,赫賽汀獲FDA批準,率先在美國上市,2002年,獲CFDA批準,在中國上市。目前,已獲批的適應癥包括:單藥用于治療HER2陽性轉移性乳腺癌;聯合紫杉醇或者多西他賽用于HER2陽性轉移性乳腺癌;HER2陽性的可手術乳腺癌患者的輔助治療;HER2陽性轉移性胃癌。在歐盟,還獲批了早期乳腺癌新輔助治療等適應癥。
曲妥珠單抗是羅氏公司的三大王牌產品之一。據該公司財報,2010年以來該品種全球銷售額一直在50億瑞士法郎(相當于50億美元)以上,且持續走高,2015年、2016年的銷售額分別達到了65.38億美元和67.82億美元。
分析人士指出,2017年,雖然已有生物類似藥參與競爭,赫賽汀市場增長仍強勁。但隨著專利期臨近,巨大的市場,也即將重新分配。中康CMH數據顯示,赫賽汀在中國的銷售份額雖不如其他國家及地區,2015年也達到16億元。
CFDA鼓勵生物類似藥研發早已布局。
2014年7月,赫賽汀在歐盟的專利已到期,美國專利也將于2019年6月到期,其生物類似藥的研發,已成為全球制藥圈的一個熱點。目前,印度(Hertraz, Mylan)、韓國(Herzuma, Celltrion)和俄羅斯(HERtiCAD, Biocad)各有一個生物類似藥上市。
在中國,近年來,生物藥市場發展快速,在很多疾病治療領域 ,優勢突出。但同時,生物藥,特別是用于惡性腫瘤等“大病”治療的生物藥,多為進口原研藥,價格高,醫保未覆蓋,可及性較差。
以赫賽汀為例,其在國內定價每支在1萬~2.5萬元人民幣之間,且在大多數省市未納入醫保目錄。
正是在這樣的背景下,早在2015年2月,CFDA就發布了《生物類似藥研發與評價技術指導原則(試行)》,鼓勵并規范本土藥企投身于生物類似藥的研發和申報。
此次,CDE征求意見的《注射用曲妥珠單抗生物類似藥臨床研究設計及審評考慮要點》,也是在上述《指導原則》)基礎上,結合該品種的特點細化仿制策略,鼓勵更多本土藥企參與研發。
健識君查詢CDE手里品種目錄發現,目前國內只有華蘭基因、正大天晴兩家企業于2014年提出了注射用曲妥珠單抗的臨床試驗,但未能查詢到進度。


新藥的專利期保護,屬于知識產權保護。新藥研發需要投入大量的時間、金錢成本,通過專利期保護,可以使其在一定時間范圍內,獨占市場,可以保護研發者的權益。
專利期到期后,仿制藥相繼上市,以其與原研藥同等的效果和價格優勢,迅速搶占市場,原研藥的銷售額會出現斷崖式下降。而原研藥持有者也不會坐以待斃。
據業內人士介紹,雖然各國《專利法》不盡相同,但專利保護的對象卻大體相同。如:根據我國《專利法(2008年修正)》第二條,產品、方法或者其改進所提出的新的方案,都在保護的范圍內。為了保持既有市場份額,或繼續開拓新的市場, 原研藥持有企業,往往會在藥品專利到期前,開發出升級版藥品,或為藥品開發、申請新的適應癥,重新申請專利,相當于”延續“了自家王牌產品的專利獲益期。
查詢CDE受理品種目錄可發現,從2011年起,羅氏就注射用曲妥珠單抗提交了一系列的補充申請。
據此,分析人士認為,本土企業/機構投身于曲妥珠單抗的生物類似藥研究之前,還應審慎多維度評估。
編輯:Shirley
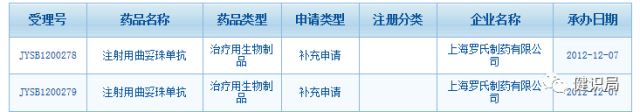
附:2011年以來,羅氏圍繞赫賽汀的補充申請情況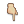
2011年
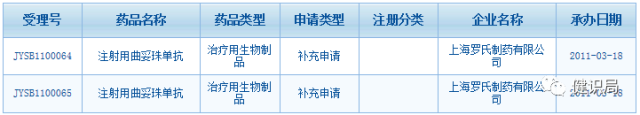
2012年
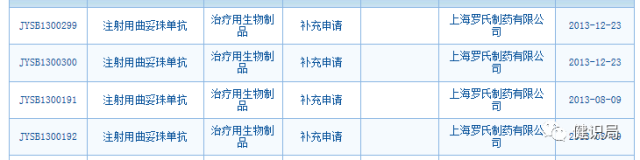
2013年

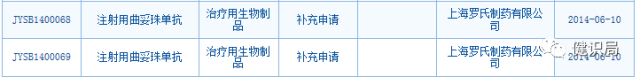
2014年

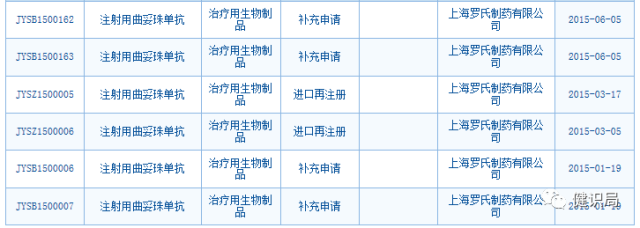
2015年

2016年

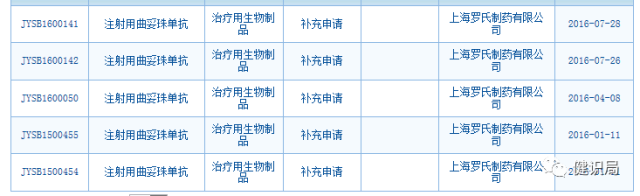
2017年

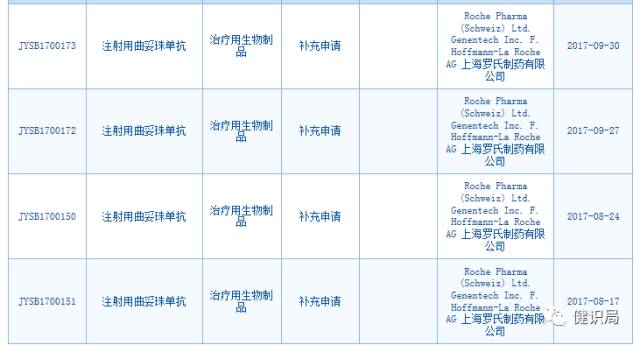
信息來源:健識局
|