剛剛,醫藥代表備案CFDA版出爐!變化大:藥企最好自建代表隊伍學術推廣(附全文標紅版)……
日期:2017/12/27

2017年12月22日晚7時許,國家食品藥品監督管理總局以及國家衛計委同時在官方網站掛出消息,就“醫藥代表登記備案管理辦法”(以下簡稱“辦法”)正式面向社會公開征求意見,共計五大章節二十條內容。備受關注的醫藥代表登記備案管理辦法終于“千呼萬喚始出來”。
可以說,從年初至歲末,自2017年重磅政策文件《國務院辦公廳關于進步一步改革藥品生產流通使用政策的若干意見》明確提出了“建立醫藥代表備案登記制度”以來,關于醫藥代表備案的關注熱度就從來沒有消退過。贊同者有之,質疑者有之,圍觀看熱鬧的亦紛紛云云。但隨著各項政策不斷明晰以及各地配套行動不斷展開,建立醫藥代表備案制的必要性以及合理性已經無需贅言。人們更關心的,實際上集中在以下幾點:
1、備案主體是誰?都要備案哪些信息?在哪里備案?對于備案代表有哪些具體要求?
2、醫藥代表備案制的出臺,究竟會對今后醫藥產品推廣、銷售的格局產生哪些影響?
3、醫藥代表備案制施行之后,藥品推廣、銷售過程之中產生的違規行為具體由誰來擔責?如何擔責?
而如今,經過近一年的反復打磨與考量,盡管仍然是處于征求意見階段,但此次“醫藥代表備案管理辦法”的公布,已經基本可以回答上述問題。
推廣應回歸學術本位
從辦法中能夠看到,首先要明確的一點,是藥品銷售人員不屬于醫藥代表。醫藥代表是做學術的,不碰產品,不碰錢。醫藥代表的從業內容,只覆蓋學術推廣、技術咨詢、協助醫務人員合理用藥,收集反饋藥品臨床使用情況和不良反應信息。除此之外,都不是醫藥代表該做的事情。
這一區別至關重要,也是此次國家構建醫藥代表備案體系的目的所在,即整頓市場秩序,更好對醫藥代表進行管理。從國家層面而言,主要是兩層意思:第一,國家層面認可醫藥代表這一職業,也認可其在整個醫藥流通過程中所起的作用,從將該職業納入職業大典可以看出;第二,現實情況是,在中國因為醫藥代表的概念混淆、職責不清等問題,造成了醫藥流通領域出現道德、行業風氣敗壞等情況擾亂市場秩序。
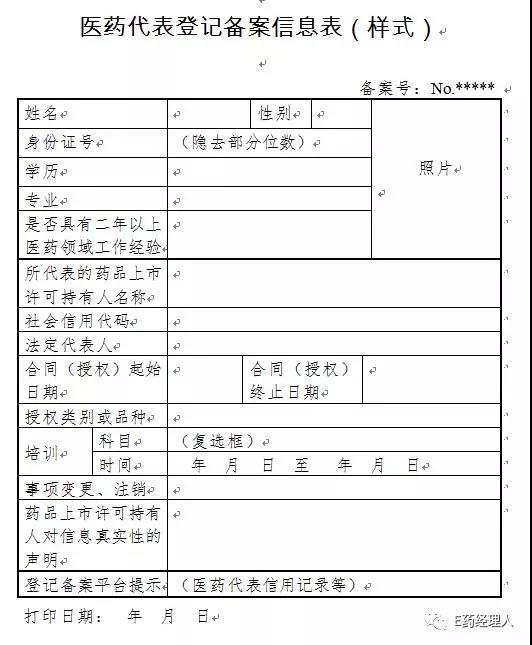
從新發布的辦法來看,醫藥代表的如下信息均需在平臺進行備案:
(一)醫藥代表的姓名、性別、照片;
(二)學歷、專業、醫藥領域從業經驗;
(三)醫藥代表的身份證號;
(四)勞動合同或授權書的起止日期;
(五)醫藥代表完成培訓情況(包括培訓科目、培訓時間);
(六)醫藥代表負責推廣的藥品類別或品種;
(七)藥品上市許可持有人的名稱、社會信用代碼、法定代表人姓名;
(八)藥品上市許可持有人對全部備案信息的真實性聲明。
而醫藥代表登記備案平臺則由國家食品藥品監督管理總局指定,由相關社會團體建設并負責維護,但同時指明,不得向藥品上市許可持有人、醫藥代表個人以及醫療機構收取費用。
其實不管是對醫藥代表進行備案登記,還是對藥品購銷領域嚴加查處,一個目的始終是清楚的,即使藥品推廣回歸至學術本位。
而新發布的方法實際上也根據實際情況作出了調整。在此前流出的對于醫藥代表登記備案的管理辦法中,醫藥代表進行備案的門檻還是比較高的,即醫藥代表需具備生命科學、醫藥衛生、化學化工相關專業的大專(含高職)及以上學歷,或雖在上述專業以外,但具備五年以上醫藥領域工作經驗。對此標準,業界普遍的聲音是“定的太高,行業現有水準達不到”,而變化在此次發布中也有所體現,即將“五年以上醫藥領域工作經驗”縮短至兩年。
總而言之,醫藥代表備案管理辦法,強調的是醫藥代表作為專業藥品學術推廣人員其身份、價值與地位,并將其與傳統意義上的“銷售代表”完全分開。
CSO危險了
從此次正式發布的“醫藥代表備案管理辦法”以及E藥經理人此前從接近此辦法制定過程的人士處所獲得的信息綜合來看,CSO行業發展受到來自醫藥代表備案制較為嚴重的影響基本已成定局。
一個不會有爭議的現狀是:至少在國家推行“兩票制”之后,CSO公司迎來了一個短暫的發展高峰。受兩票制影響,大批小分銷商、居間人被擠出了藥品流通環節,而這部分人手中所掌握的藥品進入各地醫院的渠道恰恰是CSO公司所最需要的,因此一時間上萬家CSO在全國遍地開花。
但醫藥代表備案制對其發展的最大影響在于,CSO公司在今后很有可能不再具備有資格進行學術推廣的醫藥代表。
之所以如此說,邏輯很簡單。
首先要從備案的主體來看。此前流出的非正式版“醫藥代表備案管理辦法”,將登記備案主體定義為“藥品生產企業”,而在此次最新公布的征求意見稿中,備案主體則變更為了“藥品上市許可持有人”。備案主體說法改變的同時并沒有改變備案主體的本質,通俗來講即“產品是誰家生產的,備案的主體就是誰。”在這種情況下,CSO公司明顯不具備作為主體進行備案的資格。這是必須要正確理解的第一點。
其次要看醫藥代表與備案主體之間的權責關系。作為醫藥代表登記備案的責任主體,其有責任對醫藥代表的業務行為進行負責。也就是說,凡是以企業名義在登記本案平臺上進行備案的醫藥代表,一旦出了事情企業是需要負連帶責任的。因此企業一定會對以自己為備案主體進行備案的醫藥代表進行更為嚴厲的審查,對于允許哪些人員去進行備案也會更加謹慎。在這種情況下,企業往往會優先考慮自建醫藥代表隊伍去進行學術推廣,而非委托他人如CSO公司等開展學術推廣活動,對于風險的規避,將成為在學術推廣中所考慮的第一要素。
那么CSO公司中的業務人員能否在備案平臺進行備案呢?理論上講,當然可以。從此次公布的方法來看,進行備案的醫藥代表分為兩種:一種是與藥品生產企業簽署有正式勞動合同的雇員,而另外一種則是經藥品生產企業授權開展學術推廣活動、滿足一定條件要求的人員,CSO則屬于后者。“如果企業認為,你對它(指CSO)的員工足夠信任,出了事情你愿意替他們負責,沒問題。”在一次業界大會上,接近此辦法制定過程的一位人士如此解讀,但其潛臺詞不言自明。
而更重要的是,由于CSO公司是專門做藥品代理推廣的公司,因此存在一位醫藥代表同時推廣多類產品的情況。而在多種情況下某一種產品推廣出了問題怎么辦?根據辦法,很有可能與該醫藥代表相關的所有企業都要受到牽連。“因為在備案平臺上,根據公示信息,醫藥代表跟企業是綁定的,只要你替他備案,你就要替他的行為承擔責任。”
實際上,CSO公司也確實正面臨一個越來越嚴峻的發展局面。首先是各地對于走票過票的打擊日趨嚴格,如上海市衛計委、發改委等10部門于12月19日聯合發布文件,稱將繼續重點查處非法使用發票、過票、走票、倒票等問題。盡管正規的CSO公司是以專業的學術推廣為主,但如上文所言,大量居間人、分銷商也在兩票制的影響下進入該行業,傳統的以過票走票為主的盈利模式短時間內難以完全消失。因此行業監管趨嚴下,CSO公司明顯受限。
其次,一些典型CSO公司的轉型也已經開始出現,如12月15日,泰凌醫藥宣布終止代理及推廣復旦張江旗下藥品里葆多(鹽酸多柔比星脂質體注射液)便被視為一個信號。實際上從泰凌醫藥2017年中報數據便可以看出,作為曾經國內知名的CSO公司,其第三方藥品代理業務僅剩下里葆多,當期毛利潤也僅有28.1%,占總毛利僅23%,而對比2016年CSO類業務毛利占比53.25%,權重已大幅下降。
CFDA、衛計委、行業協會,共同規范藥代行為
在整個醫藥產品的學術推廣之中,至少會涉及到四個不同的角色:醫藥代表、制藥企業、醫療機構、醫生醫務人員。根據此次公布的辦法,不管是哪一個角色出現問題,都必須承擔相應的責任。
首先對于醫藥代表來說,“醫藥代表不得承擔藥品銷售任務,不得參與統計醫生個人開具的藥品處方數量,不得直接銷售實物藥品,不得收款和處理購銷票據,不得進行商業賄賂,不得對醫療衛生機構內設部門和個人直接提供捐贈資助贊助;不得誤導醫生使用藥品,不得夸大或誤導療效,不得隱匿藥品不良反應。”在此次公布的辦法中,醫藥代表的禁止事項已經被表述得非常明確,尤其是不得銷售藥品以及不得統方,更是一直以來被一再強調的內容。
而一旦違反,醫藥代表面臨的可能是職業發展上的巨大挑戰。首先是違規行為將會被錄入登記本案平臺并向社會予以公告,并通知個人信用管理部門。其次,則要回到藥品生產企業接受至少為期一個月的脫產培訓。
對于藥品上市許可持有人來說,則不得鼓勵、暗示醫藥代表從事違規行為,不得向醫藥代表分配藥品銷售任務,不得要求醫藥代表或其他人員統計醫生個人開具的藥品處方數量,不得在登記備案中編造培訓情況或故意提供其他虛假信息。藥品上市許可持有人違反上述規定的,登記備案平臺依據食品藥品監管部門的調查結果,將其違規行為予以公示并通報信用管理部門;存在違反《反不正當競爭法》等法律法規情形的,移交相關部門依法依規查處。
對于醫療機構來說,首先要做到的,是對于醫藥代表學術推廣的行為的批準與否。根據辦法,不管是院內還是院外,只要是醫藥代表邀請醫務人員參加活動,都需要經醫療機構批準同意后方可進行。也只有按規定備案的人員可以向醫院申請去做學術推廣,醫療機構不得允許未經備案的人員開展學術推廣活動,違反相關規定的,則根據衛計委頒布的相應處罰條例來執行。這也說明,在這一點上,CFDA已經和衛計委達成了統一共識。
能夠看到的是,近年來,衛計委不斷下發文件對于醫療領域以及醫藥購銷領域中的不法現象進行治理,如2013年11月,上海市衛計委出臺“十項不得”規定;2013年12月,國家衛計委出臺“九不準”;2016年12月,湖南省衛計委出臺“五不準”;2017年1月,鄭州市衛計委出臺“六不準”,都是在政策層面進行了嚴厲管制。
引起業界最強烈反應的,則是今年9月13日上海衛計委出臺的《上海市醫藥購銷領域商業賄賂不良記錄管理規定》中,明確了醫生收受賄賂5000元以上即可被解聘并吊銷執業證書。而從目前的方法來看,這一嚴厲的措施很有可能會在更大范圍內得到延續。
而在CFDA以及衛計委之外,另一協同發揮作用的,則是行業協會。根據辦法,行業協會、學會等社會團體應發揮行業監督和自律的積極作用,鼓勵社會團體依據本辦法制定行業規范或準則,建立監督機制、信用管理機制和懲罰措施。
附件
醫藥代表登記備案管理辦法(試行)
(征求意見稿)
第一章 總 則
第一條 為規范醫藥代表的從業行為,促進醫藥產業的健康有序發展,依據《中共中央辦公廳、國務院辦公廳印發〈關于深化審評審批制度改革鼓勵藥品醫療器械創新的意見〉的通知》(廳字〔2017〕42號)和《國務院辦公廳關于進一步改革完善藥品生產流通使用政策的若干意見》(國辦發〔2017〕13號),制定本辦法。
第二條 本辦法所稱醫藥代表,是指代表藥品上市許可持有人(持有藥品批準文號的企業,下同)在中華人民共和國境內從事藥品信息傳遞、溝通、反饋的專業人員。進口藥品總代理商可以代理境外藥品上市許可持有人負責醫藥代表的登記備案管理工作。藥品銷售人員不屬于醫藥代表,不納入本辦法管理。
第二章 從業內容與資格
第三條 醫藥代表從業活動的具體內容包括:學術推廣,技術咨詢,協助醫務人員合理用藥,收集、反饋藥品臨床使用情況和藥品不良反應信息等。
醫藥代表可以通過以下形式與醫務人員溝通:
(一)在醫療機構當面溝通;
(二)舉辦學術會議、講座;
(三)提供學術資料;
(四)通過互聯網溝通或電話會議;
(五)醫療機構同意的其他形式。
從事學術推廣等活動前,應由藥品上市許可持有人向醫療機構提出申請(或發出院外活動邀請),獲得醫療機構批準同意后方可進行。
第四條 醫藥代表登記備案應當有具備以下條件之一:
(一)生命科學、醫藥衛生、化學化工相關專業的大專(含高職)及以上學歷(詳見對“相關專業”的說明);
(二)第(一)項以外的專業大專(含高職)以上學歷,且具有二年以上醫藥領域工作經驗。
藥品上市許可持有人應與醫藥代表簽訂勞動合同或授權書,勞動合同或授權書中應寫明工作崗位為醫藥代表;醫藥代表須經過崗前業務培訓,以滿足藥品上市許可持有人對醫藥代表的崗位能力要求。
第五條 藥品上市許可持有人應對醫藥代表進行業務培訓,設定崗位能力要求和培訓科目,如實撰寫培訓記錄。藥品上市許可持有人可以委托社會機構開展業務培訓,藥品上市許可持有人對培訓記錄的真實性負責。
培訓科目中應包含法律法規、職業道德教育、醫藥學專業知識、產品相關知識等內容。
鼓勵相關社會機構制定細化的培訓標準或方案,向藥品上市許可持有人提供高質量的醫藥代表業務培訓。
第三章 登記備案信息
第六條 藥品上市許可持有人是登記備案主體,應當依本辦法對其聘用(或授權)的醫藥代表在統一的平臺上進行登記備案。
第七條 醫藥代表登記備案平臺由國家食品藥品監督管理總局指定。平臺公示醫藥代表的登記備案信息,以及違規(或失信)的企業或醫藥代表的信息。
藥品上市許可持有人在登記備案平臺上按規定填寫醫藥代表的登記備案信息,完成登記備案的醫藥代表由登記備案平臺配給備案號。登記備案平臺的具體操作細則在平臺上另行公布。
第八條 登記備案平臺可由相關社會團體建設并負責維護,但不得向藥品上市許可持有人、醫藥代表個人以及醫療機構收取費用。
第九條 藥品上市許可持有人應在平臺上填寫的登記備案信息包括:
(一)醫藥代表的姓名、性別、照片;
(二)學歷、專業、醫藥領域從業經驗;
(三)醫藥代表的身份證號;
(四)勞動合同或授權書的起止日期;
(五)醫藥代表完成培訓情況(包括培訓科目、培訓時間);
(六)醫藥代表負責推廣的藥品類別或品種;
(七)藥品上市許可持有人的名稱、社會信用代碼、法定代表人姓名;
(八)藥品上市許可持有人對全部備案信息的真實性聲明。
第十條 本辦法第九條所列的(一)—(八)項備案信息(隱去個人身份證號碼的部分位數)和備案號向社會公示。醫藥代表應在登記備案平臺中下載打印個人備案信息,交由醫療機構查驗核對。
食品藥品監管部門和衛生計生部門有權限查驗以上全部信息。
第十一條 醫藥代表不再從事相關工作或終止勞動關系、停止授權的,藥品上市許可持有人應在20個工作日內完成醫藥代表的登記備案信息注銷。
藥品上市許可持有人被取消相關資質的,其備案的醫藥代表信息自資質取消之日起自動失效。
第十二條 食品藥品監管部門可對行政區域內上市許可持有人的醫藥代表的登記備案信息組織不定期核查,醫藥代表與相關企業應當配合核查。
食品藥品監管部門可委托負責運維登記備案平臺的社會團體等進行信息核查。
第四章 從業要求
第十三條 醫藥代表應如實提供登記備案信息,依法依規從業。醫藥代表在醫療機構的從業活動應公開進行,并遵守衛生計生部門的有關規定。
第十四條 藥品上市許可持有人負責對信息進行審核、錄入、變更、注銷,確保所登記備案信息的真實準確,負責所聘用(或授權)的醫藥代表的業務管理,對醫藥代表開展誠信教育和業務培訓,確保其從業行為符合相關規定。
第十五條 醫藥代表不得承擔藥品銷售任務,不得參與統計醫生個人開具的藥品處方數量,不得直接銷售實物藥品,不得收款和處理購銷票據,不得進行商業賄賂,不得對醫療衛生機構內設部門和個人直接提供捐贈資助贊助;不得誤導醫生使用藥品,不得夸大或誤導療效,不得隱匿藥品不良反應。
醫藥代表違反上述規定的,登記備案平臺依據食品藥品監管部門或衛生計生部門的查處結果,將其違規行為予以公示,并通報個人信用管理部門;食品藥品監管部門責令藥品上市許可持有人對該醫藥代表實施脫產培訓,脫產培訓至少為期一個月。醫藥代表的行為如違反法律法規規定的,依照相關法律法規追究責任。
第十六條 藥品上市許可持有人不得鼓勵、暗示醫藥代表從事違規行為,不得向醫藥代表分配藥品銷售任務,不得要求醫藥代表或其他人員統計醫生個人開具的藥品處方數量,不得在登記備案中編造培訓情況或故意提供其他虛假信息。
藥品上市許可持有人違反上述規定的,登記備案平臺依據食品藥品監管部門的調查結果,將其違規行為予以公示并通報信用管理部門;存在違反《反不正當競爭法》等法律法規情形的,移交相關部門依法依規查處。
第十七條 醫療機構不得允許未經備案的人員在醫療機構內部開展學術推廣等相關活動,醫務人員不得參與未經醫療機構批準同意的學術推廣等活動,不得違規接受社會捐贈資助,不得向醫藥代表或相關企業人員提供醫生個人開具的藥品處方數量,不得違規私自采購使用藥品。
第十八條 行業協會、學會等社會團體應發揮行業監督和自律的積極作用,鼓勵社會團體依據本辦法制定行業規范或準則,建立監督機制、信用管理機制和懲罰措施。
第五章 附 則
第十九條 對登記備案條件中“相關專業”的說明:“生命科學、醫藥衛生、化學化工相關專業的大專(含高職)及以上學歷”是指《普通高等學校高等職業教育(專科)專業目錄(2015年)》中的醫藥衛生大類、藥品制造類、化工生物技術、藥品生物技術專業大專(含高職)學歷;《普通高等學校本科專業目錄(2012年)》中的醫學門類、化學類、生物科學類、化工與制藥類、生物醫學工程類、生物工程類本科及以上學歷。
上述專業以外,培養方向與醫藥相關的其他專業(必修科目中包含醫學門類下相關課程),可在登記備案信息中注明,例如“管理學(醫藥相關)”。
專業目錄如修訂后以上專業的稱謂發生調整的、或在國外院校主修專業與以上所列舉的專業近似但稱謂不同的,應酌情予以認可。
第二十條 本辦法自2018年 月 日起施行。
信息來源:E藥經理人
|